
- 温医首页 | 加入收藏 | English
- Plos Biology|我院赵东栋副研究员揭示突触蛋白参与自闭症谱系障碍的新机制
- 作者: 编辑:王思瑶 来源: 浏览:; 时间:2025年04月15日 08:50
-
2025年4月1日,温州医科大学老年研究院院长宋伟宏院士团队赵东栋副研究员与厦门大学张云武教授合作在国际生物学领域极具影响力的1区Top期刊《Plos Biology》发表了题为“Mdga2 deficiency leads to an aberrant activation of BDNF/TrkB signaling that underlies autism-relevant synaptic and behavioral changes in mice”的研究论文,首次揭示了突触相关蛋白(MAM domain containing glycosylphosphatidylinositol anchor 2,MDGA2)在自闭症谱系障碍(Autism Spectrum Disorder,ASD)发病中的全新机制。该研究不仅深入剖析了MDGA2缺失如何引发与ASD相关的突触功能异常和行为改变,还发现通过靶向神经突触信号通路在分子层面进行调节,有望为ASD的治疗提供全新的靶点,为未来相关研究和临床治疗带来了新的曙光。

自闭症谱系障碍(ASD)是一种复杂的神经发育障碍,通常起病于儿童早期,其主要特征包括社交互动能力减弱、重复刻板行为增加以及认知功能异常。遗传学研究已发现多个与ASD相关的基因,其中大多数基因(如SHANKs、NRXNs和NLGNs等)编码突触蛋白,这表明突触功能障碍可能是ASD的主要病因。近期研究在ASD患者中发现了MDGA2蛋白的功能缺失突变和错义突变,包括覆盖MDGA2蛋白MAM结构域的截短突变和V930I突变。有研究表明,MDGA2蛋白主要表达在神经突触,能够抑制兴奋性突触的活性,但是关于MDGA2缺陷导致ASD发生的分子机制尚不清楚。
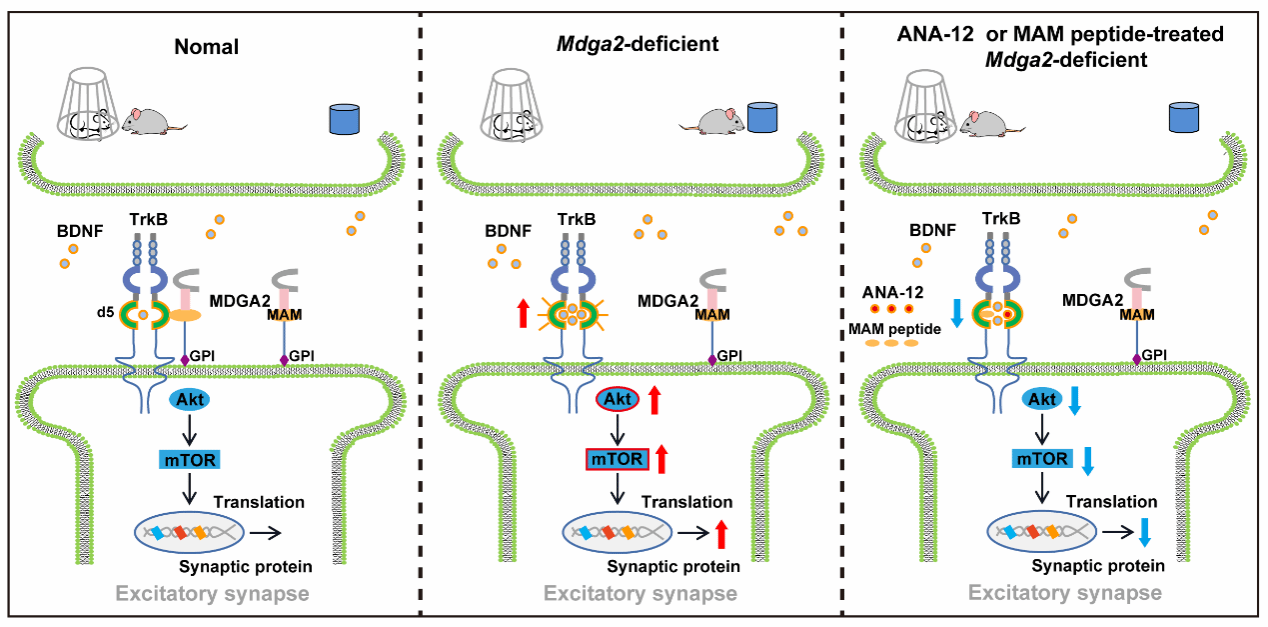
在本项研究中,团队首次发现MDGA2与受体酪氨酸激酶(Tropomyosin receptor kinase B,TrkB)相互作用,抑制脑源性神经营养因子(Brain-Derived Neurotrophic Factor,BDNF)与TrkB的结合及其下游信号通路。当MDGA2缺失时,BDNF/TrkB信号通路异常激活,导致兴奋性突触蛋白过量表达,引起ASD相关行为缺陷。通过使用MDGA2衍生多肽抑制BDNF与TrkB的结合,以及使用TrkB抑制剂ANA-12,能够显著改善MDGA2缺陷小鼠的自闭样行为障碍。
该研究揭示了MDGA2缺失引发ASD的重要分子机制,并突显了抑制BDNF/TrkB信号通路作为治疗ASD的潜在应用价值。
我院赵东栋副研究员是本研究的第一作者和共同通讯作者,该研究得到了我院院长宋伟宏院士的大力支持。
原文链接:https://journals.plos.org/plosbiology/article?id=10.1371/journal.pbio.3003047
浙ICP备12004924号 访问量统计:0021230202
